- Услуги
- Цена и срок
- О компании
- Контакты
- Способы оплаты
- Гарантии
- Отзывы
- Вакансии
- Блог
- Справочник
- Заказать консультацию
Заказать консультацию
Теоретические основы метода абсорбционной спектрофотометрии
Применение метода абсорбционной спектрофотометрии основано на способности соединений, содержащих хромофорные или ауксохромные группы поглощать электромагнитное излучение.
Хромофором (др.-греч. χρоμα – цвет и φέρω – несу) называют ненасыщенную группу атомов, обуславливающую цвет химического соединения и способную избирательно поглощать электромагнитное излучение. Введение в молекулу ауксохромных групп (от др.-греч. αὔξω – увеличиваю, χρоμα – цвет), таких, как амино- или гидроксогруппа, способствует усилению окраски.
Эти группы атомов могут выполнять функции донора (гидроксо-, амино-, метоксигруппа, вторичная аминогруппа, третичный атом азота) или акцептора (нитрогруппа, карбоксильная группа, простая и сложноэфирная группы) электронов.
Наличие в молекуле таких фрагментов обуславливает способность молекулы к избирательному поглощению электромагнитного излучения в видимой или ультрафиолетовой области спектра.
В зависимости от длины волны поглощаемого света различают абсорбционную УФ- спектрофотометрию (вещество поглощает монохроматическое излучение в определенной узкой волновой области, чаще всего –от 190 до 380 нм) и спектрофотометрию в видимой области (поглощается немонохроматическое излучение в области 380-780 нм).
Поглощение определенных квантов энергии, связанное с электронными переходами, характеризуется наличием полос поглощения в электронных спектрах атомов или молекул. Природа этих полос одинакова для ультрафиолетовой и видимой области спектра. Она обусловлена количеством и расположением электронов, способных к поглощению электромагнитного излучения. Если вещество способно к поглощению света только в УФ-области, визуально оно воспринимается как бесцветное.
Рассмотрим процесс поглощения электромагнитного излучения подробнее. Представим, что через кювету, заполненную раствором с анализируемым веществом, пропускают луч света интенсивностью I0. Испытуемый раствор поглощает электромагнитное излучение, и на выходе мы получаем луч с меньшей интенсивностью, которую обозначим как I.
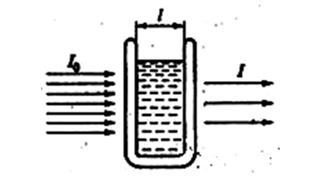
Рисунок 1. Явление поглощения веществом электромагнитного излучения
Разделив интенсивность света, прошедшего через вещество (I)на интенсивность света, падающего на вещество (I0), получим показатель, который называют пропускаемостью (Т). Десятичный логарифм обратной величины пропускаемости называют поглощением (обозначают буквой А – от «абсорбция»), или используют термины «оптическая плотность» (обозначают буквой D) либо экстрикция (обозначают буквой Е).
Разделив величину поглощения (А) на произведение концентрации вещества, выраженной в граммах на литр (С), и длины слоя поглощения в сантиметрах (b), получим величину поглощаемости (а).
Если же при расчете мы выразим концентрацию в граммах на 100 мл, а толщину слоя примем за 1 см, полученная величина будет носить название удельный показатель поглощения (Е1%1см). Таким образом, Е1% 1см = 10×a. Удельный показатель поглощения часто используют для расчета количественного содержания вещества в образце.
Графическое выражение зависимости отношения оптической плотности к длине волны называют спектром поглощения. Область интенсивной абсорбции на этом графике называют полосой или максимумом светопоглощения, а соответствующую этой области длину волны (λmax) – аналитической. В спектрах поглощения может быть один или несколько максимумов, которые соответствуют различным типам электронных переходов.
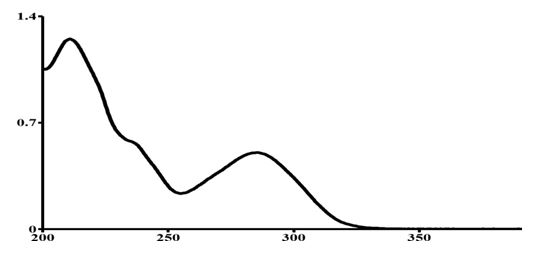
Рисунок 2. Спектр поглощения водного раствора карбамазепина
Если поглощение вызывается определенной группой атомов, и его характер мало изменяется с изменением остальной части молекулы, его называют характеристическим. По наличию характеристических полос поглощения в спектре вещества можно сделать вывод о наличии в его структуре определенных структурных элементов, сделав, таким образом, вывод о строении соединения.
Рисунок спектра зависит также от растворителя, поведения вещества в растворе (образование внутримолекулярной водородной связи, например) наличия в составе молекулы заместителей. Все эти факторы способны изменить интенсивность светопоглощения и сместить максимум в сторону длинных или коротких волн. Кроме смещения возможно появление эффекта увеличения (гиперхромный) или уменьшения (гипохромный) интенсивности светопоглощения.
По этой причине растворы для анализа изготавливают в одних и тех же условиях, а в качестве «холостого» раствора обычно используют растворитель, оптическую плотность которого «обнуляют» перед снятием спектра.
(Макиева М.С., Морозов Ю.А., Морозова Е.В., Морозов В.А. Оптические методы анализа лекарственных средств, ИПЦ Сев. Осет. гос. ун-т им. К. Л. Хетагурова)
Статьи по теме
- Рамановская спектроскопия
- Применение БИК-спектроскопии в фармацевтическом анализе
- Строение и принцип работы БИК-спектрометра
- Применение ИК-спектроскопии в фармацевтическом анализе
- Порядок работы на ИК-спектрометре
- Строение и принцип работы ИК-спектрометра
- Инфракрасная спектроскопия
- Порядок работы на фотоэлектроколориметре
- Фотоэлектроколориметрия
Полезные статьи









Узнайте цену услуг:
Узнай цену консультации
"Да забей ты на эти
дипломы и экзамены!”
(дворник Кузьмич)

